الکترولیز آب یکی از روشهای کلیدی و پاک برای تولید هیدروژن بهعنوان سوختی تجدیدپذیر و بدون کربن است. این فرآیند به دلیل پتانسیل بالایی که در کاهش انتشار کربن دارد، به یکی از ارکان اصلی تولید هیدروژن سبز تبدیل شده است. هیدروژن سبز میتواند بهعنوان جایگزینی برای سوختهای فسیلی عمل کرده و به کاهش انتشار گازهای گلخانهای کمک کند. در این فرآیند، انرژی الکتریکی مولکولهای آب را در بستر الکتروکاتالیستها به هیدروژن (H₂) و اکسیژن (O₂) تجزیه میکند. با توجه به اهمیت بالای این فناوری، میتوان آن را یکی از ابزارهای کلیدی در گذار به انرژیهای تجدیدپذیر و جایگزینی تدریجی سوختهای فسیلی دانست. (برای مطالعه مقاله فرایندها و منابع تولید هیدروژن اینجا کلیک کنید)
یکی از عوامل حیاتی در این فرآیند، استفاده از کاتالیستهاست. الکتروکاتالیستها موادی هستند که به تسریع واکنشهای الکتروشیمیایی کمک میکنند و بدون آنها، فرآیند الکترولیز با کارایی و سرعت کمتری انجام میشود. در این فرآیند، دو واکنش اصلی وجود دارد: تولید هیدروژن (HER [1]) در کاتد و تولید اکسیژن ([2] OER) در آند. انتخاب الکتروکاتالیست مناسب، نه تنها بازدهی فرآیند را افزایش میدهد، بلکه میتواند هزینهها و مصرف انرژی را نیز کاهش دهد.
فلزات گرانبهایی مانند پلاتین (Pt) و ایریدیوم (Ir) به عنوان الکتروکاتالیستهای بسیار کارآمد شناخته شدهاند. این فلزات به دلیل خواص الکتروشیمیایی خود، بهترین عملکرد را در کاهش افت پتانسیل (overpotential) نشان میدهند. با این حال، هزینه بالای این فلزات و کمیابی آنها، کاربرد وسیع صنعتی را محدود کرده است. بنابراین، پژوهشها به سمت توسعه کاتالیستهای مبتنی بر فلزات ارزانتر و بهبود عملکرد آنها در تولید هیدروژن و اکسیژن سوق یافته است.
تعریف الکتروکاتالیستها و افت پتانسیل: واکنشهای HER و OER
الکتروکاتالیستها یا همان الکترودهای کاتالیستی (کاتد و آند) نقش مهمی در تسریع واکنشهای الکتروشیمیایی دارند. در الکترولیز آب، دو واکنش اصلی وجود دارد:
- واکنش تولید هیدروژن (HER) در کاتد
- واکنش تولید اکسیژن (OER) در آند
هر دو واکنش به الکتروکاتالیست نیاز دارند تا سرعت و بازدهی آنها افزایش یابد.
در واکنش HER، مولکولهای آب یا یونهای هیدروژن در سطح الکتروکاتالیست جذب شده و با دریافت الکترون، هیدروژن آزاد میشود. این واکنش از نظر ولتاژ مصرفی نسبت به OER کمتر است. واکنش OER پیچیدهتر بوده و نیاز به چهار مرحله انتقال الکترون دارد تا یک مولکول اکسیژن تولید شود. این انتقال چندمرحلهای باعث میشود که واکنش OER به انرژی بیشتری نیاز داشته باشد.
افت پتانسیل یا اورپتانسیل
افت پتانسیل (overpotential) به معنای اختلاف بین ولتاژ ایدهآل و ولتاژ واقعی مورد نیاز برای انجام واکنشها در سیستم الکترولیز است. این افت پتانسیلها (پلاریزاسیون یا اورپتانسیل) شامل پلاریزاسیون اهمی، فعالسازی و غلظتی هستند که هر کدام از این افت ها در محدوده جریان خاصی اهمیت بیشتری دارند و غالب می شوند و عمدتا دلایل سینتیکی دارند. این موضوع یکی از چالشهای اساسی در هر دو واکنش HER و OER است که منجر به افزایش مصرف انرژی و کاهش کارایی فرآیند میشود. به همین دلیل، الکتروکاتالیستها باید بهگونهای طراحی شوند که افت پتانسیل را کاهش داده و بازدهی واکنشها را افزایش دهند.
مواد مختلف الکتروکاتالیستی
پژوهشهای متعددی برای توسعه مواد جدید بهعنوان الکتروکاتالیستهای موثر در واکنشهای HER و OER انجام شده است. در اینجا به برخی از این مواد اشاره میکنیم:
- نیکل و آلیاژهای آن:
نیکل (Ni) به دلیل هزینه پایین و فعالیت کاتالیستی بالا، یکی از پرکاربردترین فلزات واسطه در الکتروکاتالیستها است. ترکیب نیکل با فلزات دیگری مانند مولیبدن (Mo) یا آهن (Fe) فعالیت کاتالیستی آن را بهبود میبخشد. آلیاژهایی مانند NiMo و NiFe با ساختارهای نانویی متخلخل، سطح بیشتری برای واکنش فراهم میکنند و بازدهی بالاتری در کاهش افت پتانسیل دارند.
- پروسکایتها:
پروسکایتها (Perovskites) موادی با ساختار بلوری خاص هستند که بهدلیل پایداری و قابلیت تنظیم الکترونی، بهعنوان الکتروکاتالیستهای مؤثر در واکنشهای OER شناخته میشوند. پروسکایتهای مبتنی بر عناصر واسطه به دلیل فعالیت کاتالیستی بالا و افت پتانسیل کم در محیطهای قلیایی مورد توجه قرار گرفتهاند.
- کالکوژنیدهای فلزات واسطه:
کالکوژنیدهای فلزات واسطه مانند سولفیدها (Sulfides) و سلنیدها (Selenides) به دلیل رسانایی الکتریکی بالا و پیوندهای فلز-فلز قوی، بهعنوان الکتروکاتالیستهای موثر در هر دو واکنش HER و OER شناخته میشوند. بهعنوان مثال، نیکل سلنید (Ni₃Se₂) در قالب نانوساختارهای مختلف مانند نانومیلهها و فیلمها، کاتالیست بسیار کارآمدی است.
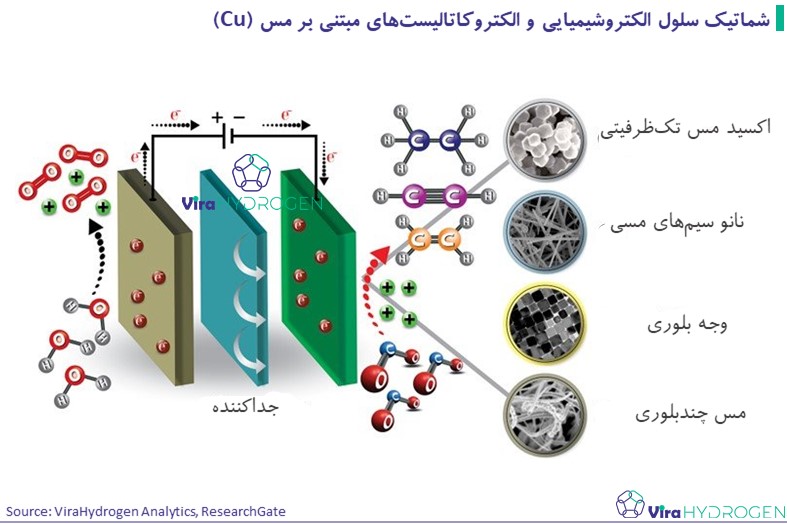
شکل زیر نمایی شماتیک از یک سلول الکتروشیمیایی و الکتروکاتالیستهای مختلف مبتنی بر مس را نشان میدهد که در فرآیند کاهش الکتروشیمیایی دیاکسید کربن (CO₂RR [3]) مورد استفاده قرار میگیرند. در این سیستم، الکترودهای کاتدی و آندی به وسیله یک جداکننده [4] از هم جدا شدهاند که وظیفه آن انتقال یونها بین الکترودهاست. انواع مختلف الکتروکاتالیستهای مسی شامل اکسید مس یکظرفیتی [5]، نانو سیمهای مسی [6]، وجههای بلوری خاص [7] و مس چندبلوری [8] در این شکل به نمایش درآمدهاند. هر کدام از این ساختارها به دلیل خواص سطحی و بلوری متفاوت، در تسریع واکنشهای کاهش دیاکسید کربن و افزایش کارایی الکتروشیمیایی نقش کلیدی دارند. بهویژه، نانوسیمهای مسی و ساختارهای بلوری، به دلیل سطح بالاتر و سایتهای فعال بیشتر، توانایی بیشتری در واکنشهای کاتالیستی از خود نشان میدهند.
روشهای بهبود عملکرد الکتروکاتالیستی
برای بهبود عملکرد الکتروکاتالیستها و کاهش افت پتانسیل، چند روش کلیدی مورد استفاده قرار میگیرد:
- ادغام با زیرلایههای رسانا:
یکی از روشهای موثر برای بهبود عملکرد الکتروکاتالیستها، ادغام آنها با زیرلایههای رسانا مانند گرافن و نانولولههای کربنی (CNTs) است. این زیرلایهها به دلیل هزینه پایین، رسانایی بالا و یکپارچگی ساختاری، بهطور گسترده در واکنشهای OER و HER استفاده میشوند.
- دوپینگ اتمی:
دوپینگ اتمی، یعنی افزودن اتمهای فلزات واسطه به ساختار الکتروکاتالیستها، یکی دیگر از روشهای بهبود عملکرد است. دوپینگ با اتمهایی مانند کبالت (Co)، آهن (Fe) و منگنز (Mn) میتواند رسانایی الکتریکی اکسیدهای فلزی را بهبود بخشد و دسترسی به سایتهای فعال را افزایش دهد.
- استفاده از مواد آمورف:
مواد آمورف به دلیل داشتن نقصهای سطحی یا Surface Defects بیشتر و ساختار نامنظم، سایتهای فعال بیشتری برای واکنش فراهم میکنند. این نقصها سطح تماس واکنشدهندهها با کاتالیست را افزایش میدهد و در نتیجه فعالیت کاتالیستی را بهبود میبخشد. بهعنوان مثال، فیلمهای آمورف کبالت سلنید [1] در واکنش HER عملکرد بهتری نشان داده و افت پتانسیل را کاهش دادهاند.
نتیجهگیری
الکتروکاتالیستها نقش حیاتی در واکنشهای تولید هیدروژن و اکسیژن از طریق الکترولیز آب دارند. استفاده از فلزات واسطه و مواد جایگزین بهجای فلزات گرانبها، امکانپذیری این فرآیند را در مقیاس بزرگ و با هزینه کمتر فراهم میکند. بهبود عملکرد الکتروکاتالیستها از طریق ادغام با زیرلایههای رسانا، دوپینگ اتمی و استفاده از مواد آمورف به کاهش افت پتانسیل و افزایش بازدهی واکنشها منجر میشود. این پژوهشها مسیرهای جدیدی برای تولید هیدروژن بهعنوان منبع انرژی پاک و پایدار فراهم میکنند و چشماندازهای امیدوارکنندهای برای آینده انرژی تجدیدپذیر ارائه میدهند.
[1] Cobalt Selenide(CoSe)
[1] Hydrogen Evolution Reaction
[2] Oxygen Evolution Reaction
[3] Carbon Dioxide Reduction Reaction
[4] Separator
[5] Cuprous oxide
[6] Cu nanowire
[7] Crystal facet
[8] Polycrystalline Cu