در دهههای اخیر، هیدروژن (H₂) و به طور ویژه هیدروژن سبز به عنوان یکی از مهمترین و پایدارترین جایگزینهای سوختهای فسیلی معرفی شده است. عدم انتشار آلایندههای زیست محیطی از جمله کربن دی اکسید، امکان یکپارچگی و استفاده از انرژیهای تجدیدپذیر در فرایند تولید هیدروژن سبز مبتنی بر الکترولیز آب یکی از مزایا اصلی توسعه زنجیره ارزش هیدروژن سبز در صنایع مختلف است. اما همچنان چالشهای جدی در بهرهوری و هزینههای تولید هیدروژن سبز وجود دارد.
در الکترولیز آب دو نیمواکنش اصلی وجود دارد: واکنش تکامل هیدروژن ([1] HER) و واکنش تکامل اکسیژن (OER [2]) برای تسریع در واکنش OER برای تسریع این واکنش نیاز به کاتالیستهای کارآمد وجود دارد. در حال حاضر، کاتالیستهای مبتنی بر فلزات گرانبها مانند پلاتین، ایریدیوم و روتنیوم به عنوان مؤثرترین کاتالیستها شناخته میشوند، اما هزینه بالا و کمبود منابع این فلزات استفاده تجاری از آنها را محدود کرده است. برای غلبه بر این چالشها، توسعه الکتروکاتالیست های خودایستا (FSECs [3]) با استفاده از مواد ارزانتر و فراوانتر، به عنوان یک راهحل امیدوارکننده معرفی شده است.
برای مطالعه مقاله “بررسی روند بهبود الکتروکاتالیست ها در واکنشهای الکترولیز آب برای تولید هیدروژن” اینجا کلیک کنید
معرفی الکتروکاتالیست های خودایستا
این نوع کاتالیستها شامل موادی هستند که به طور مستقیم و در محل روی بسترهای رسانا بدون نیازی به هیچ ماده افزودنی از جمله چسبها تشکیل میشوند. برخلاف کاتالیستهای معمول که به یک بستر پشتیبان نیاز دارند، الکتروکاتالیستهای خودایستا از مزایای زیر برخوردار هستند:
- پایداری مکانیکی بالا: ساختار پایدار، مقاومت کاتالیستها را در برابر خوردگی و فرسایش به طرز چشمگیری افزایش میدهد.
- انتقال مؤثر الکترون و یونها: عدم استفاده از مواد چسبنده، به کاتالیستها این امکان را میدهد که بار الکتریکی را سریعتر انتقال دهند و کارایی واکنشهای الکتروشیمیایی را افزایش دهند.
- افزایش سطح فعال کاتالیست: ساختار سهبعدی این مواد سطح بسیار بیشتری را برای انجام واکنشها فراهم میکند که در نتیجه باعث افزایش نرخ واکنش میشود.
الکتروکاتالیستهای خودایستا به دلیل عدم نیاز به پشتیبان اضافی، نسبت به الکتروکاتالیستهای معمول بار الکتریکی را سریعتر منتقل کرده و سطح بیشتری از ماده فعال را برای واکنشها فراهم میکنند. این ویژگیها باعث بهبود عملکرد آنها در تولید هیدروژن و واکنشهای الکتروشیمیایی میشود.
در سالهای اخیر، برای ساخت الکتروکاتالیستهای خودایستا از فلزات ارزانتر مانند آهن (Fe)، کبالت (Co)، نیکل (Ni) و منگنز (Mn) استفاده شده است. الکتروکاتالیستهای ساخته شده از این فلزات به دلیل خواص فیزیکی و شیمیایی منحصربهفرد، فعالیت بالا، پایداری شیمیایی، هزینه پایین، گزینههای مناسبی برای جایگزینی فلزات گرانبها هستند.بهویژه، فلزاتی مانند نیکل و کبالت به دلیل فعالیت کاتالیستی بالایشان در واکنشهای OER و HER بهعنوان جایگزینهای مناسبی برای پلاتین و ایریدیوم شناخته میشوند. به کارگیری این فلزات میتواند بهطور قابلتوجهی هزینه تولید کاتالیستها را کاهش دهد، بدون اینکه کارایی بهطور چشمگیری کاهش یابد.
در شکل زیر شماتیکی از ساختار الکتروکاتالیستهای خودایستا به تصویر کشیده شده است. این ساختار شامل بستری متخلخل کاتالیستی است که مواد فعال کاتالیستی بهصورت مستقیم روی آن تشکیل شدهاند. تصویر همچنین نحوه رشد الکتروکاتالیستها روی بسترها، بدون نیاز به چسب یا افزودنی، و استفاده از سطح فعال بالا برای تسریع واکنشهای الکتروشیمیایی را نشان میدهد.
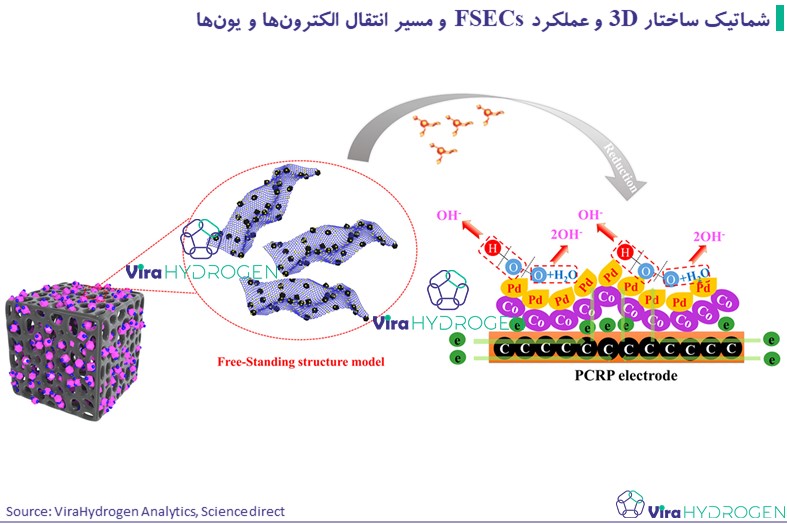
ساختار و مزایای الکتروکاتالیست های خودایستا
الکتروکاتالیستهای خودایستا بر اساس ساختار سهبعدی کوچک یا Micro-spatial-stereo construction طراحی شدهاند. این ساختارها دارای ویژگیهایی هستند که کارایی کاتالیستها را به طور قابل توجهی افزایش میدهند، از جمله:
- سطح فعال گسترده: ساختار سهبعدی و متخلخل این مواد باعث افزایش سطح تماس آنها با مواد واکنشدهنده میشود.
- افزایش پایداری مکانیکی: ساختارهای سهبعدی باعث افزایش مقاومت مکانیکی کاتالیستها در برابر تغییر شکل و فرسایش میشود.
- انتقال سریعتر الکترون و یونها: طراحی این ساختارها به گونهای است که کانالهای مناسبی برای انتقال سریع الکترون و یونها فراهم میکنند، که منجر به افزایش کارایی واکنشهای الکتروشیمیایی میشود.
مواد رسانا در این الکتروکاتالیستها نقش حیاتی دارند. این مواد نه تنها امکان انتقال سریع الکترونها را فراهم میکنند، بلکه به دلیل سطح ویژه بالای آنها، قابلیت افزایش سایتهای واکنشی را نیز دارند. برخی از رایجترین بسترهای رسانا عبارتند از:
- فومهای فلزی: فومهای نیکل، مس و آهن به عنوان بسترهای رسانا در بسیاری از الکتروکاتالیستهای خودایستا استفاده میشوند. این فومها با ساختار متخلخل خود سطح وسیعی برای واکنشهای الکتروشیمیایی فراهم میکند.
- پارچه کربنی و کاغذ فیبر کربنی: به دلیل رسانایی بالا و وزن سبک، این مواد به عنوان بسترهای مناسبی برای رشد مواد فعال کاتالیستی در الکتروکاتالیستهای خودایستا به شمار میروند.
چالشها و راهکارهای توسعه
با وجود مزایای فراوان، توسعه الکتروکاتالیستهای خودایستا با چالشهایی روبرو است. یکی از چالشهای مهم نیاز به پتانسیلهای بالاتر نسبت به کاتالیستهای فلزات گرانبها است. برای غلبه بر این مشکل، استفاده از آلیاژهای فلزی و ترکیبات چند فلزی میتواند به بهبود خواص الکتروشیمیایی کمک کند. همچنین، پایداری الکتروکاتالیستها در طول زمان از موضوعات اساسی است. راهکارهایی مانند استفاده از پوششهای مقاوم به خوردگی یا مواد دارای پایداری شیمیایی بالا میتواند به افزایش دوام آنها منجر شود.
کاربردهای الکتروکاتالیست های خودایستا
الکتروکاتالیست های خودایستا به دلیل ویژگیهای ساختاری و عملکردی منحصر به فرد خود، در حوزههای مختلفی از جمله تولید هیدروژن، ذخیرهسازی انرژی و فناوریهای الکتروشیمیایی کاربرد دارند. برخی از این کاربردها عبارتاند از:
- الکترولیز آب: الکتروکاتالیستهای خودایستا به طور گستردهای در الکترولیز آب برای تولید هیدروژن به کار میروند. در این فرآیند، واکنش OER (تولید اکسیژن در آند) و واکنش HER (تولید هیدروژن در کاتد) با استفاده از الکتروکاتالیستها تسریع میشوند.
- سلولهای سوختی: در سلولهای سوختی، الکتروکاتالیستهای خودایستا به عنوان مواد الکترودی عمل میکنند که واکنشهای اکسایش-کاهش در آند و کاتد را تسریع میکنند. این واکنشها به تولید برق از طریق سوخت هیدروژن یا سایر سوختها منجر میشوند.
- باتریهای فلز-هوا: در باتریهای فلز-هوا، الکتروکاتالیستها نقش حیاتی در واکنشهای اکسایش فلز و کاهش اکسیژن دارند. الکتروکاتالیستهای خودایستا با افزایش سطح فعال و کاهش مقاومت الکتریکی میتوانند کارایی این باتریها را بهبود بخشند.
الکتروکاتالیستهای خودایستا به دلیل ویژگیهای ساختاری پیشرفته، پایداری بالا و سطح فعال گسترده، همچنان یکی از حوزههای مهم تحقیقاتی در فناوریهای الکتروشیمیایی محسوب میشوند. با تمرکز بر بهینهسازیهای آتی در استفاده از مواد جایگزین و بهبود طراحیهای سهبعدی، کارایی این فناوری افزایش یافته و هزینهها به طور قابلملاحظهای کاهش خواهد یافت. این امر، کاهش هزینه های تولی هیدروژن را در پی خواهد داشت.
مراجع
[1] Hydrogen Evolution Reaction
[2] Oxygen Evolution Reaction
[3] Free‑Standing Eletrocatalysts (FSECs)